Tempo de leitura: [rt_reading_time] minutos.
O metabolismo ósseo e do eixo PTH-Cálcio-Fósforo-Vitamina D é uma das principais complicações da doença renal crônica (DRC). Apesar de pequenas alterações estarem presentes desde as fases iniciais da DRC, é a partir do estágio IIIb que elas se acentuam e estão universalmente presentes quando o paciente estiver prestes a iniciar diálise (estágio V). Este ano, a The Kidney Disease: Improving Global Outcomes (KDIGO) publicou novas diretrizes para diagnóstico e tratamento da doença óssea no paciente renal crônico (Diagnosis, Evaluation, Prevention, and Treatment of Chronic Kidney Disease–Mineral and Bone Disorder: Synopsis of the Kidney Disease: Improving Global Outcomes 2017 Clinical Practice Guideline Update).
No nosso texto, vamos utilizar a publicação no Annals of Internal Medicine focada no paciente adulto não transplantado. Também iremos chamar a doença óssea de CKD-MBD, que é o termo mais utilizado na literatura em substituição ao antigo “osteodistrofia renal”.
A que se refere o texto?
CKD-MBD engloba um conjunto de alterações nos níveis séricos de cálcio, fósforo, vitamina D, FGF 23 (fibroblast growth factor 23) e/ou PTH que pode levar a alterações no turnover ósseo, mineralização, crescimento e força com consequente risco de fratura, dores e/ou calcificação extravascular.
Como o processo ocorre?
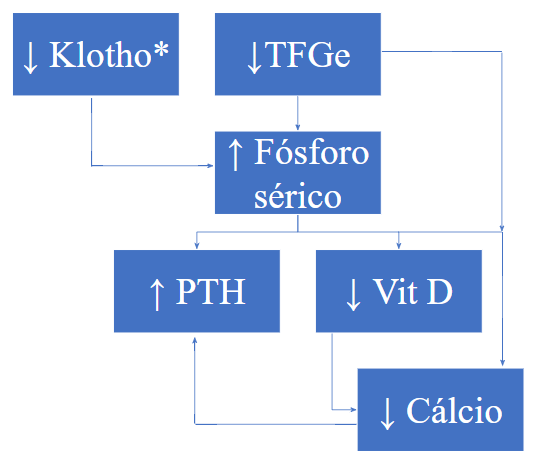
A partir das alterações apresentadas na Figura 1, no paciente com DRC a compensação é insuficiente à medida que ocorre perda progressiva da função renal. Mesmo sob estímulo, o fósforo continua a ser excretado de modo insuficiente, há hiperfosfatemia, hipocalcemia e hipovitaminose D. Neste ponto, há dois caminhos possíveis:
- PTH aumenta → deformidades ósseas → osteíte fibrosa cística. É a forma mais comum, o hiperparatireoidismo secundário, chamado de “high turnover”.
- Resistência ao PTH → redução formação matriz óssea colágena e óssea. É a chamada forma “low turnover ou adynamic bone disease” (doença óssea adinâmica).
Há ainda outras formas de doença óssea, como osteomalácia e formas mistas, mas menos comuns na prática clínica. Também pode ocorrer da hiperplasia da paratireóide se tornar autônoma e haver um hiperparatireoidismo terciário, no qual o PTH aumenta progressivamente e sem supressão pelo cálcio/fósforo séricos; neste caso, o tratamento é cirúrgico, a paratireoidectomia.
Qual a consequência clínica?
- Dores ósseas
- Fraturas patológicas
- Deformidades
- Cardiotoxicidade
- Acredita-se que o aumento do duplo produto cálcio x fósforo promova lesão celular, dano endotelial, hipertrofia do miocárdio e, principalmente, calcificação vascular, potencializando as consequências da aterosclerose prematura e contribuindo para a DRC ser um “equivalente” de IAM e AVC como preditor do risco cardiovascular.
Como diagnosticar e tratar?
O diagnóstico é feito pela dosagem bioquímica de cálcio, fósforo, PTH e vitamina D. É recomendado na diretriz o monitoramento periódico em todo paciente com DRC destes parâmetros bioquímicos bem como realização de densitometria óssea a partir do estágio 3a até o 5D (diálise).
Até 2013, o PTH era usado como divisor de águas entre a forma “high turnover” (osteíte fibrosa cística, PTH elevado) e a “low turnover” (doença óssea adinâmica, PTH normal ou baixo, em geral < 100 pg/ml). Contudo, trabalhos recentes mostraram que não há um ponto de corte universal e a nova diretriz sugere a avaliação sequencial o PTH.
- PTH subindo + hiperfosfatemia + hipocalcemia → considere high turnover
- PTH platô ou decrescendo + cálcio normal/alto → considere low turnover
Propõe-se ainda o uso de biomarcadores de atividade de remodelamento ósseo, como fosfatase alcalina óssea e procollagen type-1 N-terminal propeptide (p1NP), porém a diretriz não endossa nenhum deles na prática clínica. O que pode ser necessário é a biópsia óssea, pouco usada na prática clínica, mas o padrão-ouro para diferenciar as formas de CKD-MBD.
Considerando os riscos da hiperfosfatemia e seu papel como “precursora” / ponto de partida fisiopatológico, durante muitos anos recomendou-se o tratamento precoce da hiperfosfatemia, mesmo em fases iniciais da doença. A ideia era dar carbonato de cálcio, que quela o fosfato, reduz sua absorção, e ainda fornece o cálcio, associado ou não à vitamina D. Dessa forma, estaríamos corrigindo as alterações laboratoriais antes das consequências clínicas, evitando o excesso de PTH.
Mas o tiro saiu pela culatra…
Dados recentes mostram que o uso de cálcio como quelante e a vitamina D ativa podem causar hipercalcemia, exacerbando a calcifilaxia e o depósito vascular, com maior risco cardiovascular!
Por isso, a diretriz atual recomenda tratar apenas se houver hiperfosfatemia, dando preferências à dieta e aos quelantes sem fósforo (como o sevelamer). A diretriz não determina valores exatos, mas na literatura recomenda-se tratar quando fósforo > 4,5 mEq/L (não dialisa) ou > 5,5 mEq/L (dialisa). Há, ainda, um grupo de autores que só recomenda o tratamento com quelantes de fósforo nos pacientes em diálise, pois é o grupo que se beneficiou nos estudos.
Além disso, a reposição de cálcio e a vitamina D devem ser reservados para o paciente com hiperparatireoidismo secundário importante. As evidências para este tratamento são melhores no paciente que já dialisa do que naqueles ainda em tratamento conservador. A diretriz não determina valores específicos, mas a literatura recomenda tentar manter PTH < 150 pg/ml sem deixar o cálcio > 9,5 mg/dl. O cálcio pode ser reposto na forma de análogo, o cinacalcet, e a vitamina D na sua forma ativa, o calcitriol. Ambos estão melhor baseados em evidências no paciente em diálise.
Não há, ainda, consenso no tratamento da osteoporose nestes pacientes, e a diretriz recomenda “considerar” terapia antireabsortiva, leia-se bifosfonatos.
E a doença adinâmica? Menos comum, é recomendado suspender reposição de cálcio e vitamina D. A ideia é deixar concentração sérica de cálcio cair para tentar subir os níveis de PTH! Exatamente o oposto do hiperparatireoidismo!
Tenha em mãos informações objetivas e rápidas sobre práticas médicas. Baixe o Whitebook.
Referências:
- Ketteler M, Block GA, Evenepoel P, Fukagawa M, Herzog CA, McCann L, et al. Diagnosis, Evaluation, Prevention, and Treatment of Chronic Kidney Disease–Mineral and Bone Disorder: Synopsis of the Kidney Disease: Improving Global Outcomes 2017 Clinical Practice Guideline Update. Ann Intern Med. [Epub ahead of print 20 February 2018] doi: 10.7326/M17-2640
- http://kdigo.org/wp-content/uploads/2017/02/2017-KDIGO-CKD-MBD-GL-Update.pdf
- Babayev, R. and Nickolas, T. L. (2015), Bone Disorders in Chronic Kidney Disease: An Update in Diagnosis and Management. Semin Dial, 28: 645–653. doi:10.1111/sdi.12423







