A terapia com fluidos faz parte do dia a dia na UTI, seja para utilização na forma de expansão volêmica, soluções de manutenção, ou diluição de medicações. No entanto, ainda não temos uma resposta definitiva sobre a melhor solução a ser utilizada, cloreto de sódio 0,9% (SF 0,9%) ou soluções balanceadas (Ringer Lactato / Plasma-lyte®).
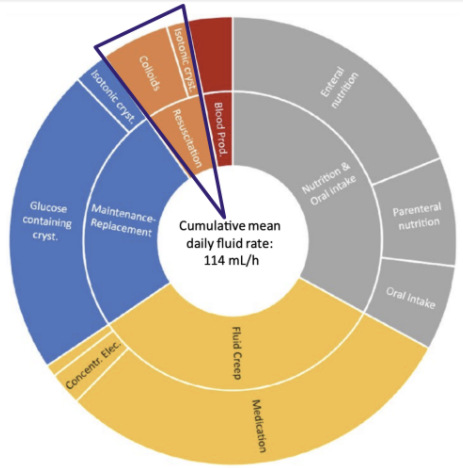
Apesar de algumas vezes ser o centro das discussões, os bolus de expansão com fluidos representam uma pequena parte do volume total de fluidoterapia recebida pelos pacientes na UTI¹. Assim, os estudos mais recentes dão grande importância às outras formas de fluidos que o paciente recebe durante a internação.

Estudo
Há muito tempo se advoga a redução da utilização do SF 0,9%, em favor das soluções balanceadas, em grande parte pelo excesso de cloreto em sua composição, que promove a ocorrência de acidose metabólica hiperclorêmica, e possivelmente aumento de lesão renal aguda (LRA) e mortalidade. Isso lhe rendeu o apelido de “soro anti fisiológico”4. Apesar do racional fisiológico, seria necessário a avaliação do impacto das diferentes soluções em desfechos clínicos centrados no paciente.
Leia também: Os prejuízos do excesso de sódio no ambiente intra-hospitalar

Alguns estudos como o SALT-ED³ e SMART2, demonstraram que o uso de soluções balanceadas promoveu uma redução do “major adverse kidney events within 30 days” (MAKE30), que engloba morte, necessidade de diálise, ou disfunção renal persistente (aumento de creatinina acima de 2x o valor basal). No entanto, ambos estudos foram unicêntricos, realizados na Universidade de Vanderbilt (EUA).
Enquanto isso, o estudo SPLIT, multicêntrico, realizado pela ANZICS (Australian and New Zealand Intensive Care Society), não encontrou nenhuma diferença na incidência de lesão renal aguda, independente da solução utilizada.
O estudo BaSICS (brasileiro) e o estudo PLUS (ANZICS) foram construídos para tentar esclarecer essa questão.
O BaSICS foi financiado pelo Ministério da Saúde brasileiro, com apoio da Baxter® para fornecimento dos fluidos e auxílio logístico. Ele apresentou um desenho fatorial, buscando responder duas dúvidas:
- As soluções balanceadas são superiores ao SF 0,9%?
- Se realizada expansão volêmica, uma infusão “lenta” (333 mL/h) é superior a uma infusão “rápida” (999 mL/h)?
Desenho do estudo
O estudo foi multicêntrico, envolvendo 75 centros brasileiros, com inclusão de 11.000 pacientes. Uma façanha gigantesca, capaz de ser realizada por poucos, e ainda por cima em meio a pandemia de Covid-19.
Essa amostra foi calculada com intenção de obter poder de 89% para observar uma redução da mortalidade em 90 dias de 35% (no grupo controle) para 31.5% no grupo solução balanceada (HR 0.90, com erro α de 0.05).
Foram incluídos pacientes com necessidade de pelo menos uma expansão volêmica, que não tivessem expectativa de alta no dia seguinte à inclusão, e que preenchessem pelo menos um dos seguintes critérios de risco para lesão renal aguda: 1. Idade maior que 65 anos; 2. Hipotensão (PAM < 65 mmHg, PAS < 90 mmHg, ou necessidade de droga vasoativa); 3. Sepse; 4. Necessidade de ventilação mecânica invasiva ou não-invasiva por pelo menos 12h; 5. Oligúria (≤ 0.5 ml/Kg/h por 3 horas) ou elevação de creatinina ( > 1.2 para mulheres e > 1.4 para homens); 6. Cirrose ou insuficiência hepática aguda.
Foram excluídos: 1. Pacientes com LRA tratados com hemodiálise (HD) ou com expectativa de HD nas próximas 6 horas; 2. Presença de distúrbio eletrolítico grave ( sódio ≤120 ou ≥160 mmol/L); 3. Expectativa de morte nas próximas 24 horas; 4. Suspeita ou confirmação de morte encefálica; 5. Pacientes em cuidados paliativos exclusivos.
O desfecho primário do estudo foi a mortalidade em 90 dias. Desfechos secundários analisados foram: necessidade de terapia substitutiva renal em 90 dias; incidência de lesão renal aguda KDIGO 2-3 no 30 e 70 dias; dias livres de ventilação mecânica em 28 dias; e escore SOFA total e seus componentes individuais, no 30 e 70 dias.
Intervenções
Os grupos recebiam o fluido do estudo (solução balanceada ou SF 0,9%) para todas soluções de manutenção, bolus de expansão, ou diluição de qualquer medicação que precisasse de mais de 100 mL Todas embalagens eram idênticas, de forma que pacientes, médicos, e pesquisadores foram cegados para a intervenção.
Diluições em menos de 100 mL de fluidos poderiam ser feitas de acordo com as práticas locais, assim como poderiam ser administrados hemoconcentrados, bicarbonato ou albumina, se indicados pela equipe assistente, sem restrições. Na ocorrência de expansão com fluidos, a velocidade da infusão era determinada pelo alocamento do paciente nos grupos do estudo (333 mL/h ou 999 mL/h).
As características de base dos pacientes foram bem balanceadas, com idade média de 60 anos; aproximadamente 50% dos pacientes internados para cirurgias eletivas, ~12% para cirurgias não eletivas, e ~48% por motivos clínicos (~18.5% sepse). A mediana do SOFA na admissão foi de 4, com ~32% dos pacientes apresentando LRA-KDIGO I, ~60% com hipotensão, e ~44% necessidade de ventilação mecânica na admissão. Aproximadamente 4.5% das admissões foram por traumatismo cranioencefálico (TCE).
Resultados
Não houve diferença significativa no desfecho primário entre os grupos. A mortalidade em 90 dias no grupo solução balanceada foi de 26.4%, versus 27.2% no grupo SF 0,9% (HR 0.97; IC 95% 0.90-1.05; p=0.47).
Na análise do outro braço do estudo, que buscou avaliar a infusão de expansão volêmica de forma “lenta” (333 ml/h) versus “rápida” (999 mL/h), também não houve diferença no desfecho primário de mortalidade em 90 dias (HR 1.03; IC95% 0.96-1.11; p=0.46).
Também não houve diferença nos desfechos secundários de necessidade de terapia substitutiva renal em 90 dias, incidência de lesão renal aguda KDIGO 2-3 no 30 e 70 dias, ou dias livres de ventilação mecânica em 28 dias.
Lembre-se que desfechos secundários e análise de subgrupos devem ser observados apenas como dados exploratórios, com objetivo de gerar hipóteses. Dito isso, dos outros múltiplos desfechos secundários e terciários, poucas diferenças foram encontradas, provavelmente resultantes do acaso (erro alfa). Foram realizadas diversas análises de subgrupo, o que aumenta a chance desse tipo de erro.
No entanto, é interessante notar que no subgrupo de pacientes vítimas de TCE a mortalidade foi menor naqueles que receberam SF 0,9% (21.1%), comparado aos que receberam soluções balanceadas (31.3%), de forma significativa (HR 1.48; IC 95% 1.03-2.12; p=0.02). Essa hipótese havia sido levantada por uma análise post-hoc de um estudo observacional prévio5. Provavelmente nessa população o SF 0,9% será adotado como fluido de escolha, uma vez que esses pacientes foram excluídos do estudo PLUS (a ser publicado).
Alguns fatores podem ter limitado o poder do estudo para encontrar diferenças entre os grupos analisados. Primeiro, a mortalidade em 90 dias no estudo (27.2% no grupo SF 0,9%) foi menor do que o esperado (35%), provavelmente pelo grande número de internações para cirurgias eletivas. Segundo, o “standard of care” atual é de restrição de fluidos para pacientes na UTI, de modo a evitar os efeitos deletérios de um balanço hídrico excessivamente positivo.
Terceiro, parte do grupo “solução balanceada” foi contaminado pelo uso de SF 0,9% antes da admissão na UTI (no centro cirúrgico ou pronto socorro), e para diluição de medicamentos (com menos de 100 ml). No entanto, esse tipo de interferência é inerente a esse desenho de estudo, e seu controle agrega um grau de complexidade elevado na execução do trabalho. Todos esses fatores levantam a dúvida se houve exposição suficiente à terapia estudada.
Outra limitação do estudo foi a imputação de valores para os casos de “missing data”. No entanto, isso foi realizado pois já estava previsto no Plano de Análise Estatística (SAP) no estudo, publicado previamente6. Assim, a despeito da pequena quantidade de missing data, talvez menor que o previsto, os autores se mantiveram fiéis ao SAP previsto, ainda que isso significasse realizar a imputação de dados.
Saiba mais: Terapia empírica para candidíase invasiva na UTI: para quem, quando e como?
Conclusão
No estudo BaSICS, que avaliou pacientes em UTI com necessidade de expansão volêmica, o uso de soluções balanceadas em comparação com SF 0,9% não reduziu de forma significativa a mortalidade em 90 dias ou a incidência de lesão renal aguda. Esse achado difere do resultado de estudos prévios, como o SMART. O estudo PLUS, conduzido pela ANZICS, é outro trabalho de grande porte sobre o tema, que tem previsão de publicação dos resultados ainda esse ano.
Baseado na análise de subgrupos do BaSICS, o SF 0,9% talvez passe a ser o fluido de escolha para utilização em pacientes vítimas de TCE. Essa população não será avaliada no PLUS, sendo o BaSICS a melhor evidência disponível sobre o assunto nesse momento.
Como os resultados entre os diferentes estudos são conflitantes, ainda não podemos tirar conclusões definitivas sobre o tema. Após a publicação do PLUS, a realização de uma grande metanálise, incluindo os principais ensaios clínicos randomizados sobre o tema (SMART, SPLIT, BaSICS e PLUS), poderá fornecer poder estatístico suficiente para resolver essa questão de uma vez por todas.
Referências bibliográficas:
- Van Regenmortel N. Maintenance fluid therapy and fluid creep impose more significant fluid, sodium, and chloride burdens than resuscitation fluids in critically ill patients: a retrospective study in a tertiary mixed ICU population. Intensive Care Med. 2018 Apr;44(4):409-417. doi: 10.1007/s00134-018-5147-3
- SMART trial: Balanced Crystalloids versus Saline in Critically Ill Adults. N Engl J Med. 2018 Mar 1;378(9):829-839. doi: 10.1056/NEJMoa1711584
- SLAT-ED trial: Balanced Crystalloids versus Saline in Noncritically Ill Adults. N Engl J Med. 2018;378(9):819-828. doi:10.1056/NEJMoa1711586
- Kellum JA. Abnormal saline and the history of intravenous fluids. Nat Rev Nephrol. 2018 Jun;14(6):358-360. doi: 10.1038/s41581-018-0008-4.
- Rowell SE, Fair KA, Barbosa RR, Watters JM, Bulger EM, Holcomb JB, Cohen MJ, Rahbar MH, Fox EE, Schreiber MA. The Impact of Pre-Hospital Administration of Lactated Ringer’s Solution versus Normal Saline in Patients with Traumatic Brain Injury. J Neurotrauma. 2016 Jun 1;33(11):1054-9. doi: 10.1089/neu.2014.3478.
- Damiani LP, Cavalcanti AB, Biondi RS, Freitas FGR, Figueiredo RC, Lovato WJ, Amêndola CP, Serpa Neto A, Paranhos JLDR, Veiga VC, Guedes MAV, Lúcio EA, Oliveira Júnior LC, Lisboa TC, Lacerda FH, Miranda TA, Maia IS, Grion CMC, Machado FR, Zampieri FG. Statistical analysis plan for the Balanced Solution versus Saline in Intensive Care Study (BaSICS). Rev Bras Ter Intensiva. 2020 Oct-Dec;32(4):493-505. doi: 10.5935/0103-507X.20200081






